 打印本文
打印本文  关闭窗口
关闭窗口 01
CAR-T源起
下图是T细胞识别癌细胞发挥作用的机制。它主要通过自身表面的受体,也就是TCR来识别癌细胞。而这个过程中依赖于肿瘤细胞表面MHC分子对抗原分子的呈递。如果这个MHC分子出现问题,比如肿瘤细胞为实现逃逸而下调了MHC分子的表达,就会导致T细胞无法高效地识别癌细胞。
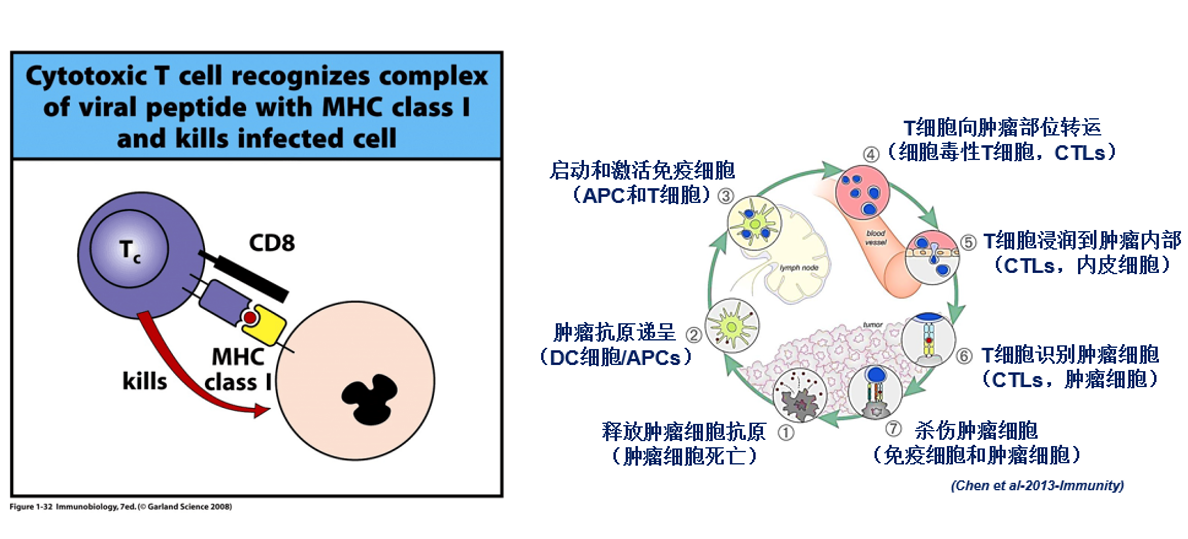
图1. 左:杀伤性T细胞通过TCR识别癌细胞进而发挥作用,右:杀伤性T细胞在肿瘤免疫反应中的作用过程
1989年,在研究T细胞受体(TCR)的过程中,以色列科学家Zelig Eshhar和他的团队发现B细胞产生的抗体和TCR结构相似,具有恒定区和可变区。抗体能够特异性识别抗原,TCR却只能识别MHC递呈的抗原片段。如果将抗体中的可变区移植到TCR的恒定区,就能够改变T细胞受体的抗原特异性,介导细胞杀伤作用。Eshhar等人将表达特定抗体的基因序列赋予细胞毒性T细胞(CTL),这项特定抗体赋予了T细胞识别半抗原――2,4,6-三硝基苯基(TNP)的能力,使得T细胞实现了抗原特异性的、非MHC限制的活化及其效应的增强。
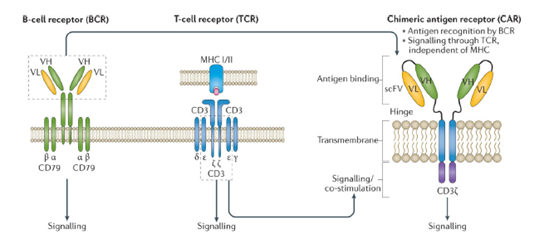
图2. 初代CAR由BCR的可变区和TCR的恒定区组成
接着,为将这项技术投入疾病治疗,Eshhar与Rosenberg实验室合作,运用来源于抗体的单链抗体片段scFv成功构建了3个不同癌症靶标的嵌合抗原受体,第一代CAR-T由此诞生。
02
药物机理
嵌合抗原受体(Chimeric Antigen Receptor,CAR)主要由三个功能域构成,分别是胞外结构域、跨膜结构域和胞内结构域。胞外结构域由负责识别并结合抗原的单克隆抗体的单链可变片段(scFv)及一段起连接作用的铰链区(Hinge)构成。胞内结构域由共刺激结构域和信号转导结构域构成。

图3. 嵌合抗原受体结构
 打印本文
打印本文  关闭窗口
关闭窗口