 打印本文
打印本文  关闭窗口
关闭窗口

图1 研究成果(图源:Nature)
两名患者在CAR-T细胞疗法10多年后,仍处于缓解状态,一直未被检测到白血病的迹象。用流式细胞仪可跨时间点检测到CAR-T细胞,定量 PCR 证实了两名患者在所有时间点都存在CTL019(靶点为CD19的CAR-T细胞)。对两名患者最近一次血液测试显示,10年后两位患者的血液中仍然可以检测到CTL019细胞(图2),分别占所有T细胞的0.8%和0.1%,而CD19+的B细胞和CLL细胞则一直处于未检测到或高度抑制状态(小于1%)。
为了探究CAR-T细胞扩增的克隆性质,研究人员通过分选CAR-T 细胞,对T细胞受体(TCR)β链库进行深度测序(TCR-seq)以及慢病毒载体整合位点(LVIS)分析。TCR-seq揭示了患者1在2.3个月和1.4年时间点之间发生的克隆转变。而患者2的克隆组成在前两年逐渐转变,总体上更加稳定。LVIS数据显示基本与TCR-seq数据中观察到的克隆转变一致。
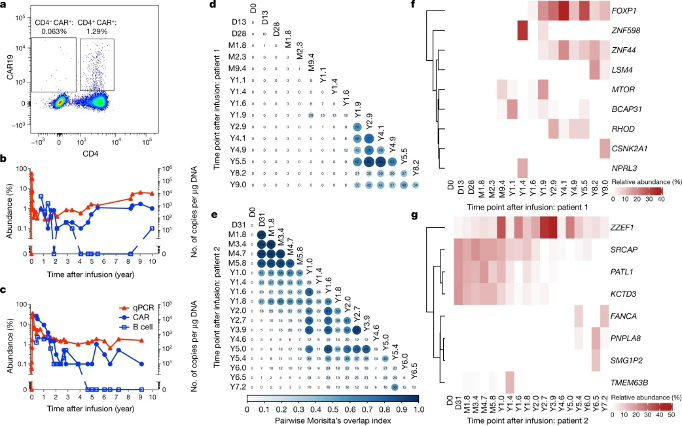
图2 CAR-T细胞疗法过程中效应物和靶点的分子追踪(图源:Nature)
研究人员开发了一个由40种抗体组成的试板,通过使用质谱流式细胞技术(CyTOF)在多个时间点分析CAR-T细胞的表型(图3)。数据显示,患者1在接受CAR-T细胞治疗后的第1.8个月,CD8+细胞占CAR-T细胞的29.3%,并在之后的时间点按比例减少。而CD4+细胞在第1.4年占CAR-T 细胞的97.5%,第3.4年到9.3年(最晚时间点)占比甚至超过了99.6%,患者2表现出总体相似的趋势。研究人员进一步研究发现,在两名患者中,CAR-T细胞治疗反应主要分为两个阶段:以CD8+ T细胞和CD4- CD8- Helioshi CAR-T细胞为代表的初始反应阶段,以及以具有增殖性和溶细胞功能的CD4+ CAR-T细胞表型为主的长期缓解期。
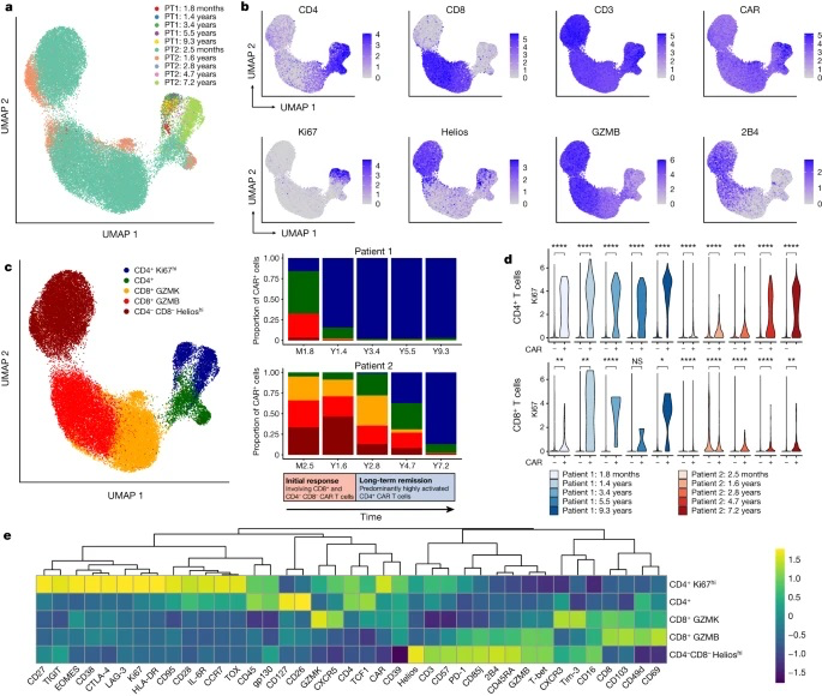
图3 使用CyTOF技术在多个时间点分析CD3 + CAR + T细胞(图源:Nature)
通过后续一系列相关实验,研究人员发现,两名患者都出现了高度活化的 CD4+群体,在后期时间点上占据了CAR-T细胞群的主导地位。这种转变反映在CAR-T细胞克隆组成的稳定上,克隆谱系由少数克隆主导。单细胞分析显示,这些长期存在的CD4+ CAR-T细胞在持续功能激活和增殖的同时表现出细胞毒性特征。
作为该研究的作者之一,CAR-T之父Carl June博士说,“在未来10年里,还可以检测到当时输注可以杀死癌细胞的CAR-T 细胞,这非常振奋人心!我们可以得出结论,CAR-T 细胞疗法确实可以治愈白血病患者”。总之,本研究详细探究了两名患者体内基于CD19靶点的CAR-T细胞的长达十年的细胞变化、功能和分子特征。这些发现有助于研究人员了解与抗癌反应和白血病长期缓解相关的CAR -T细胞特征,为患者疾病长期缓解提供了理论支持。
国内CAR-T疗法开展现状
目前全球已有7款CAR-T疗法获批上市,其中国外5款,国内2款(表1)。2021年是我国正式开启细胞免疫治疗元年,分别于6月份迎来首款CAR-T疗法―阿基仑赛注射液;9月3日,迎来第二款获批的CAR-T产品―瑞基奥仑赛注射液,这也是中国首款1类生物制品的CAR-T产品。随着这两款注射液注射液前后在中国获批上市,癌症免疫治疗领域火速掀起一阵“CAR-T热”。
表1 全球获批CAR-T疗法产品
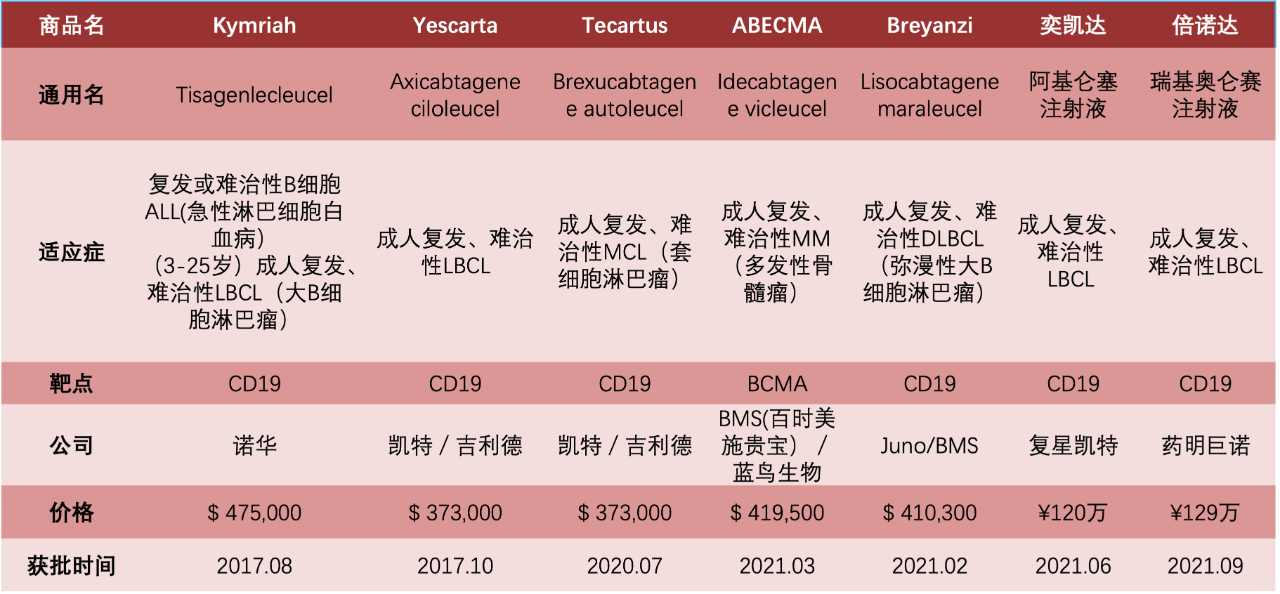
数据来源:Insight数据库|制表:生物探索编辑团队
热潮之下,针对CAR-T细胞疗法的研究还在持续加大火候。除了已经上市的阿基仑赛和瑞基奥仑赛,还有近40款CAR-T疗法正在研发(表2)。其中,诺华的CTL-019在国内已经进入III期临床试验,合源生物、南京传奇、科济生物等企业也进入了临床II期。统计发现,这些药的靶点主要布局在CD19上,其次为 BCMA。
表2 国内处于临床期的CAR-T细胞疗法

数据来源:Insight数据库|制表:生物探索编辑团队
当然CAR-T疗法虽然大火,也有其亟待突破的局限性。目前上市的CAR-T细胞产品都是针对B细胞淋巴瘤、急性淋巴细胞白血病等血液肿瘤,在实体瘤中CAR-T细胞治疗术的应用还十分有限,临床试验也多以失败告终,如何将这一颇具前景的技术运用于实体瘤的治疗,还存在许多无法解决的难题,有待科学家攻克。
阿基仑赛注射液上市后现状
国内阿基仑赛注射液的批准上市,为广大癌症患者带来了希望。据报道,在该药上市后一周,6月30日,上海交通大学医学院附属瑞金医院副院长赵维莅及其团队为患者陈阿姨开展了CAR-T治疗。该患者也成为全国首例接受CAR-T治疗的患者。经过为期2个月的治疗,原本无药可治的陈阿姨症状得到了完全的缓解,至8月26日,已出院回家休息。据复星国际联席CEO陈启宇表示,消息一经传出,一些不明真相的癌症患者蜂拥至瑞金医院,也给该医院造成了一定的困惑。
CAR-T疗法并非万能抗癌神药。武汉大学人民医院东院肿瘤科副主任章必成表示,目前国内上市的CAR-T产品并不适合所有的肿瘤患者,所获适应症范围也只针对血液肿瘤,而在大家熟悉的像肺癌、肝癌、大肠癌、乳腺癌等实体肿瘤领域,CAR-T尚未被成功运用,而临床上这些患者更多。同时,它也有一定的副作用,应用时也需要医生团队有非常丰富的处理经验。此外,据复星凯特官网介绍,奕凯达的最佳总缓解率(ORR)达到79.2%,相关数据显示客观缓解率83%、完全缓解率58%,4年总生存率达44%。
目前该疗法已在全国如上海、江苏、湖北、浙江、广东、北京等多个省市陆续开出首批处方。CAR-T细胞疗法的出现,已被符合适应症的患者视为了“救命稻草”。但120万的价格,也成为了一道高高的门槛。而在全球范围,美国同类药物价格为在37.3万美元至43万美元,折合人民币约240万-300万元。
为了实现企业盈利以及综合效益最大化,目前国内共有十几家企业在开展CAR-T相关的临床实验,复星凯特需要趁着其他对手还没起跑,尽量多收获利益以平衡成本。我国淋巴瘤发病率(约为 6.68/10万人)虽呈逐年上升趋势,但应用CAR-T治疗的患者多为难治性或复发性的B淋巴细胞瘤患者,其数量有限,为实现收益,药企也不得不使定价趋于高位。
专家表示不管是国家监管层面还是市场竞争层面,未来CAR-T的价格会有下调,但是其受限于技术成本,其价格短期仍会居于高位,但随着对于CAR-T治疗的研究不断深入,以CAR-T为主的细胞疗法有望实现“平民化”。
参考资料:
[1]Melenhorst JJ, Chen GM, Wang M, et al. Decade-long leukaemia remissions with persistence of CD4+ CAR T cells. Nature. 2022 Feb;602(7897):503-509. doi: 10.1038/s41586-021-04390-6. Epub 2022 Feb 2. PMID: 35110735.
[2]http://www.360doc.com/showweb/0/0/1018716131.aspx
[3]CAR-T上市后现状:一针120万的抗癌“神药”。https://xw.qq.com/cmsid/20211017A09NPN00?f=newdc
 打印本文
打印本文  关闭窗口
关闭窗口